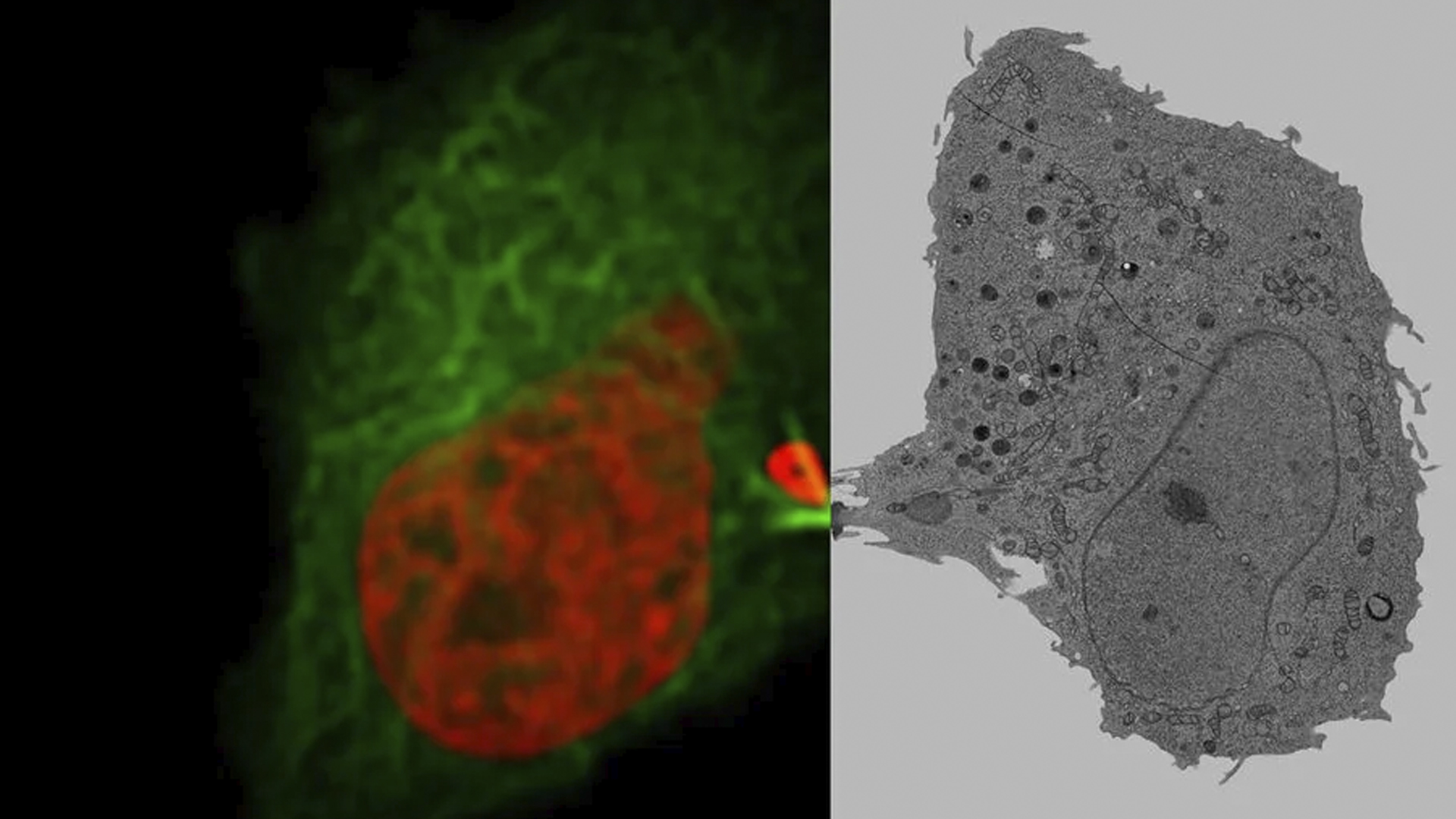
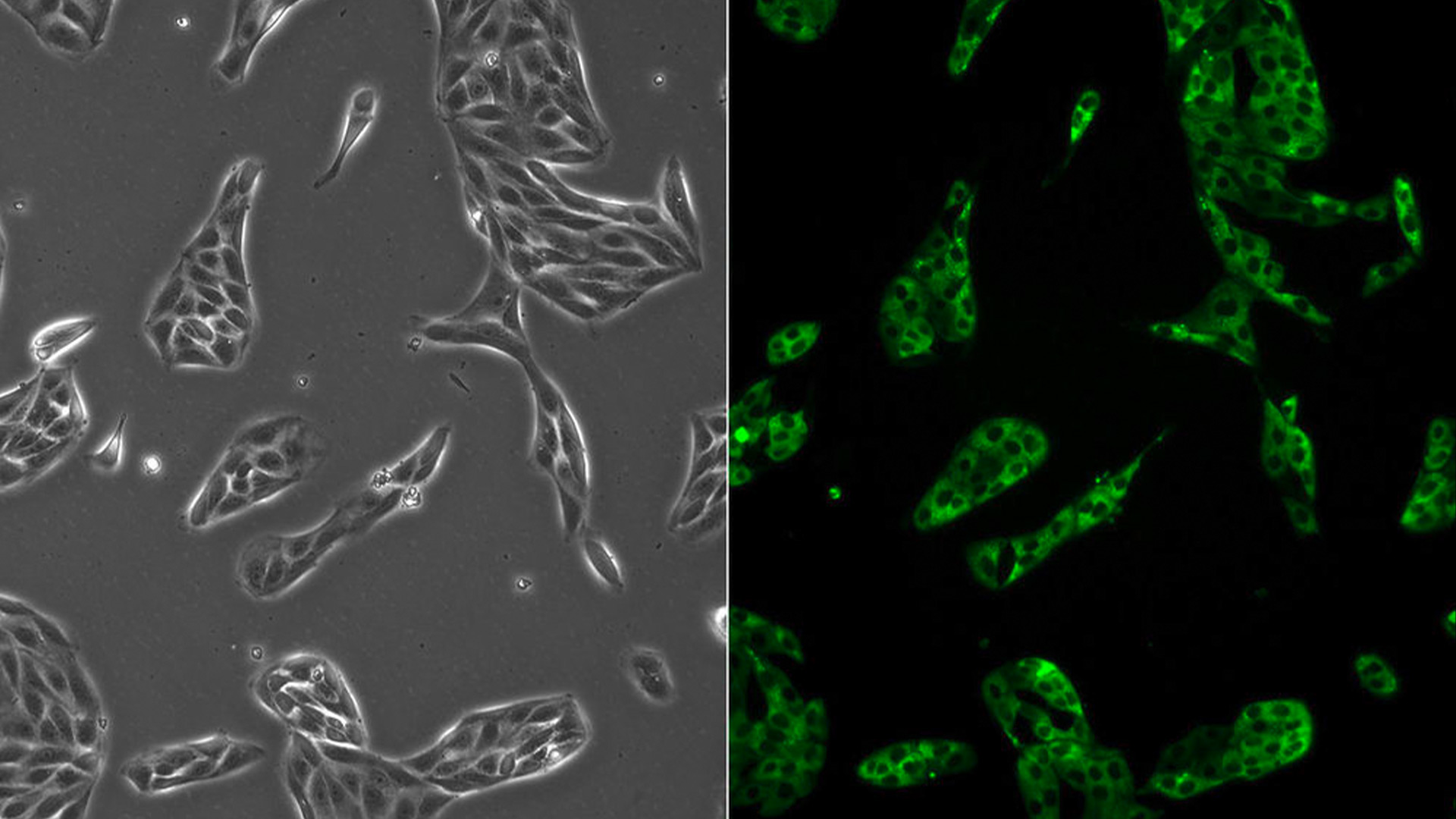
Flussi di lavoro per la preparazione dei campioni EM e i loro Usi
I ricercatori possono ottenere risultati di alta qualità, precisi e riproducibili durante l'acquisizione di campioni con la Microscopia elettronica utilizzando le soluzioni Leica per la preparazione dei campioni. Le nostre soluzioni supportano la microscopia elettronica a scansione (SEM), la Microscopia elettronica a trasmissione (TEM) e la crio EM.
I nostri esperti di imaging sono a disposizione per fornire consigli sulle soluzioni per i flussi di lavoro di preparazione dei campioni EM.
Come possono i ricercatori preparare i campioni per il SEM?
La preparazione dei campioni per la SEM (Microscopia elettronica a scansione) prevede tecniche quali il rivestimento, l'essiccazione e l'inclusione per garantire un'immagine ottimale. Utilizzando le soluzioni Leica per i campioni SEM, i ricercatori migliorano la conduttività, riducono gli artefatti e garantiscono superfici stabili e di alta qualità per un'imaging SEM affidabile a temperatura ambiente.
Quali sono i metodi migliori per la preparazione dei campioni TEM?
La preparazione dei campioni TEM (microscopia elettronica a trasmissione) richiede sezioni ultrasottili e prive di danni, rivestimento sputter di griglie EM e colorazione per ottenere una visualizzazione dettagliata della struttura. Con la precisione e l'affidabilità degli strumenti Leica, i ricercatori possono produrre immagini GST ad alta risoluzione.
Cosa è importante per la preparazione dei campioni crio-EM?
Il Cryo EM beneficia della vitrificazione mediante congelamento rapido per mantenere le strutture nel loro stato naturale.
Le soluzioni Leica per la crio-preparazione, tra cui la vetrificazione avanzata, il rivestimento, la sezione ultra sottile, la crio-pianificazione e i flussi di lavoro personalizzabili di trasferimento crio e CLEM, consentono di ottenere campioni riproducibili e privi di contaminazione. Contribuiscono a mantenere le strutture native, forniscono un targeting preciso e consentono l'imaging crio EM ad alta risoluzione.
Perché scegliere gli strumenti e le soluzioni Leica per la preparazione dei campioni EM?

Preparazione del campione SEM
Gli strumenti per la preparazione dei SEM di Leica Microsystems includono rivestimenti sputter ad alto vuoto ed essiccatori a punto critico. Queste soluzioni garantiscono immagini di superficie di alta qualità. Inoltre, gli strumenti Leica forniscono risultati coerenti e affidabili per i vostri studi SEM.

Preparazione del campione TEM
I ricercatori possono affidarsi alle soluzioni di preparazione TEM di Leica Microsystems per ottenere precisione e affidabilità. Strumenti essenziali come gli ultramicrotomi e i sistemi di colorazione automatizzati aiutano a produrre sezioni ultrasottili e immagini ad alta risoluzione. Lo Sputter coating migliora la conduttività del campione e la qualità delle immagini.

Preparazione Cryo-EM completa
Con gli strumenti di crio-preparazione di Leica Microsystems, tra cui i congelatori a tuffo e i congelatori ad alta pressione, i ricercatori assicurano un congelamento e una vetrificazione rapidi. Inoltre, il nostro sistema di trasferimento dei campioni per i flussi di lavoro criogenici offre opzioni di trasferimento per tutti i tipi di campioni. Questa opzione li protegge dalla contaminazione, garantendo un'analisi Cryo-EM accurata e dettagliata.