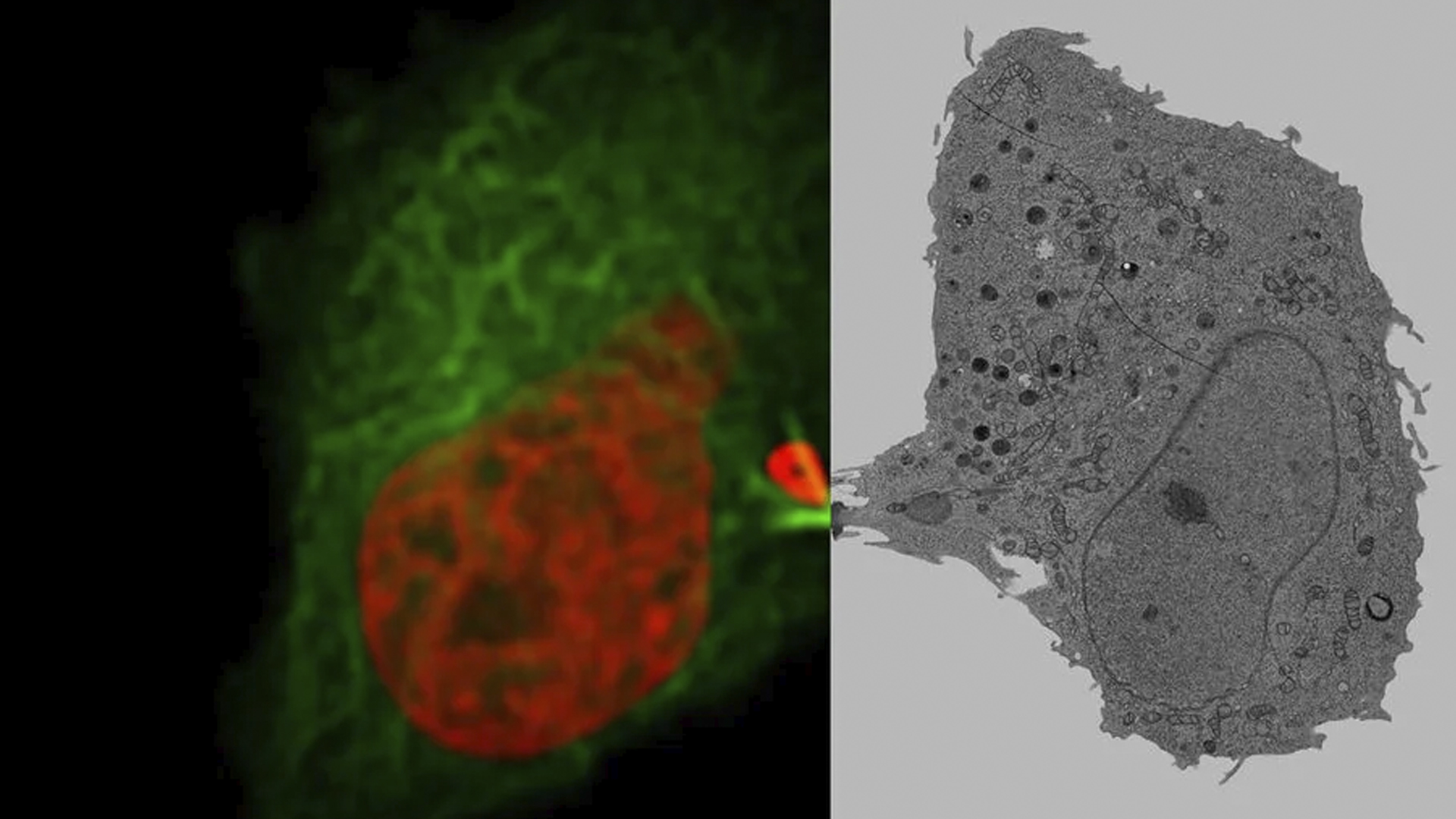
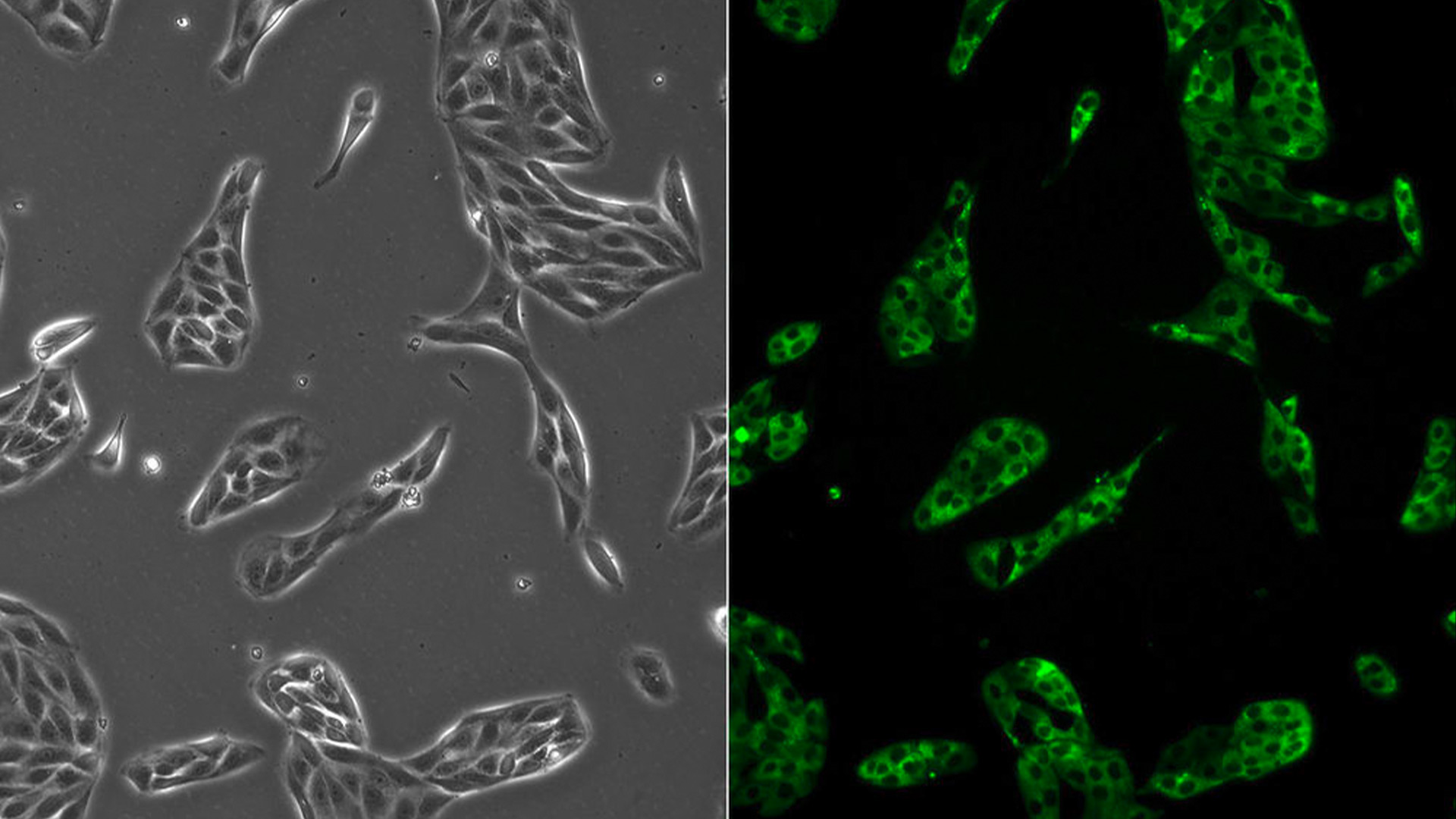
Flux de préparation des échantillons EM & Utilisations
Les solutions de préparation d'échantillons Leica permettent aux chercheurs d'obtenir des résultats de haute qualité, précis et reproductibles lors de l'imagerie d'échantillons en microscopie électronique. Nos solutions prennent en charge la microscopie électronique à balayage (MEB), la microscopie électronique à transmission (MET) et la cryomicroscopie électronique.
Nos experts en imagerie sont là pour vous aider en vous conseillant sur les solutions pour les flux de travail de préparation des échantillons EM & Uses.
Comment les chercheurs peuvent-ils préparer les échantillons pour le MEB ?
La préparation des échantillons pour la microscopie électronique à balayage (MEB) implique des techniques telles que le revêtement, le séchage et l'enrobage afin de garantir une imagerie optimale. En utilisant les solutions Leica pour les échantillons MEB, les chercheurs améliorent la conductivité, réduisent les artefacts et garantissent des surfaces stables et de haute qualité pour une imagerie MEB fiable à température ambiante.
Quelles sont les meilleures méthodes de préparation des échantillons TEM ?
La préparation des échantillons TEM (microscopie électronique à transmission) nécessite des coupes ultrafines et sans dommages, un revêtement par pulvérisation cathodique des grilles EM et une coloration pour obtenir une visualisation détaillée de la structure. Grâce à la précision et à la fiabilité des instruments Leica, les chercheurs peuvent produire des images TEM de haute résolution.
Qu'est-ce qui est important pour la préparation des échantillons de cryo-EM ?
Le Cryo EM bénéficie de la vitrification par congélation rapide pour maintenir les structures dans leur état naturel.
Les solutions Leica de préparation cryogénique - y compris la vitrification avancée, l'enrobage, la coupe ultramince, le cryoplaning et les flux de travail personnalisables de transfert cryogénique et de CLEM - fournissent des échantillons reproductibles et exempts de contamination. Ils aident à maintenir les structures natives, permettent un ciblage précis et une imagerie cryo EM à haute résolution.
Pourquoi choisir les instruments et solutions Leica pour la préparation d'échantillons EM ?

Préparation de l'échantillon pour le MEB
Les outils de préparation du MEB de Leica Microsystems comprennent des appareils de revêtement par pulvérisation cathodique sous vide poussé et des sécheurs à point critique. Ces solutions garantissent une imagerie de surface de haute qualité. De plus, les instruments Leica fournissent des résultats cohérents et fiables pour vos études MEB.

Préparation de l'échantillon TEM
Les chercheurs peuvent compter sur les solutions de préparation TEM de Leica Microsystems pour leur précision et leur fiabilité. Des outils essentiels tels que les ultramicrotomes et les systèmes de coloration automatisés permettent de produire des coupes ultrafines et des images à haute résolution. Le revêtement par pulvérisation cathodique améliore la conductivité de l'échantillon et la qualité de l'imagerie.

Préparation Cryo-EM complète
Avec les instruments de cryopréparation de Leica Microsystems, notamment les congélateurs à plongeur et les congélateurs à haute pression, les chercheurs garantissent une congélation et une vitrification rapides. En outre, notre système de transfert d'échantillons pour les flux de travail cryogéniques offre des options de transfert pour tous les types d'échantillons. Cette option les protège de la contamination, garantissant ainsi une analyse Cryo-EM précise et détaillée.