ライカのエキスパートが、電顕試料作製ワークフローとお客様のアプリケーションに適したソリューションをご提供します。
研究者はどのようにしてSEM用の試料を準備するのか?
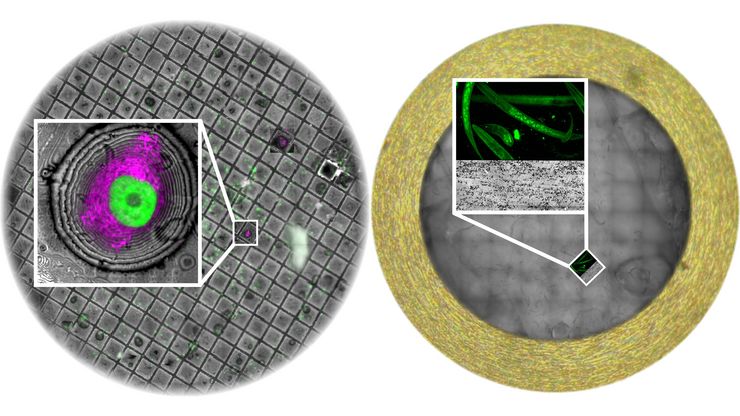
SEM(走査型電子顕微鏡)用の試料調製において、コーティング、乾燥、包埋などの技術を用いることで、最適なイメージングが実現します。SEMサンプルにライカのソリューションを使用することで、研究者は導電性を改善し、アーティファクトを低減し、室温での信頼性の高いSEMイメージングのための安定した高品質の試料面を保つことができます。
TEMサンプルの前処理にはどのような方法が最適ですか?
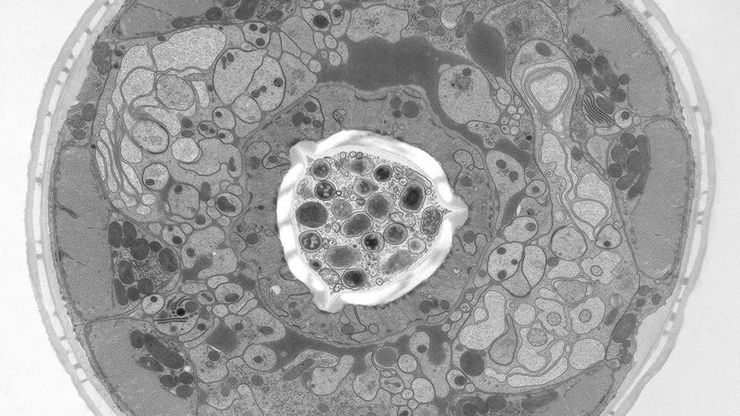
TEM(透過型電子顕微鏡)の試料作製には、超薄切片、損傷のない切片、EMグリッドのスパッタコーティング、および詳細な構造の可視化するための染色が必要になります。ライカの装置の精度と信頼性により、研究者は高解像のTEM画像を撮影することができます。
クライオ電子顕微鏡 (CryoEM)のサンプル前処理で重要なことは何ですか?
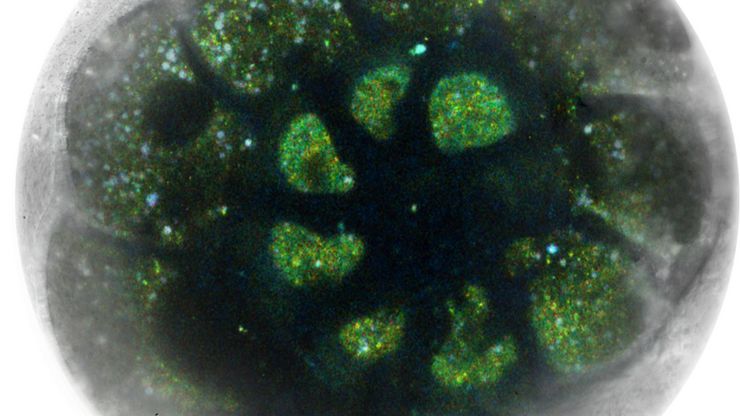
急速凍結により非晶質化することで、試料の構造を自然の状態に保つことができます。
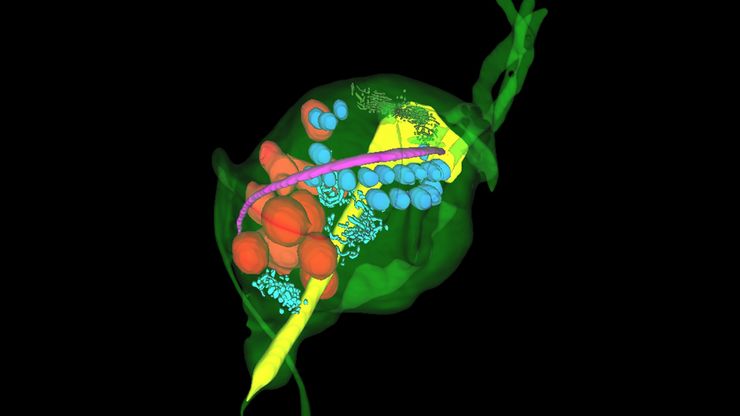
ライカのクライオ試料作製ソリューションは、高度な非晶質化、コーティング、超薄切片化、クライオ下での断面出し、カスタマイズ可能なクライオトランスファーとCLEMワークフローを備えており、再現性が高くコンタミのない試料作製を実現します。試料本来の構造を維持することで正確なターゲティングが可能になり、高解像の Cryo EMイメージングを実現します。
電顕試料作製にライカの装置とソリューションを選ぶ理由とは?
電顕試料作製ワークフローとアプリケーションに関するよくある質問
患者の安全が最優先です。従って、致死量に関する知識は非常に重要であり、臨床試験を検討する前に規制当局から要求されるのです。生死判別アッセイを用いることで、閾値を評価することが可能となります。十分な量のデータを効率的に取得するために、Micaは最適なソリューションです。
高精度に組織領域を回収することで、高品質のゲノムおよびプロテオーム解析を可能にします。レーザーマイクロダイセクションは、バイオ医薬品研究者が特定の細胞や組織領域をターゲットとし、医薬品開発においてより正確でコンタミネーションのない研究を促進するのに役立ちます。
顕微鏡観察は、化合物や薬剤候補に対する細胞応答の詳細な空間的知見を得るのに役立ちます。創薬段階、すなわち生細胞培養モデルや組織の品質管理や反応経路の詳細な分析には、さまざまな創薬・開発ニーズに対応するライカ製品があります。