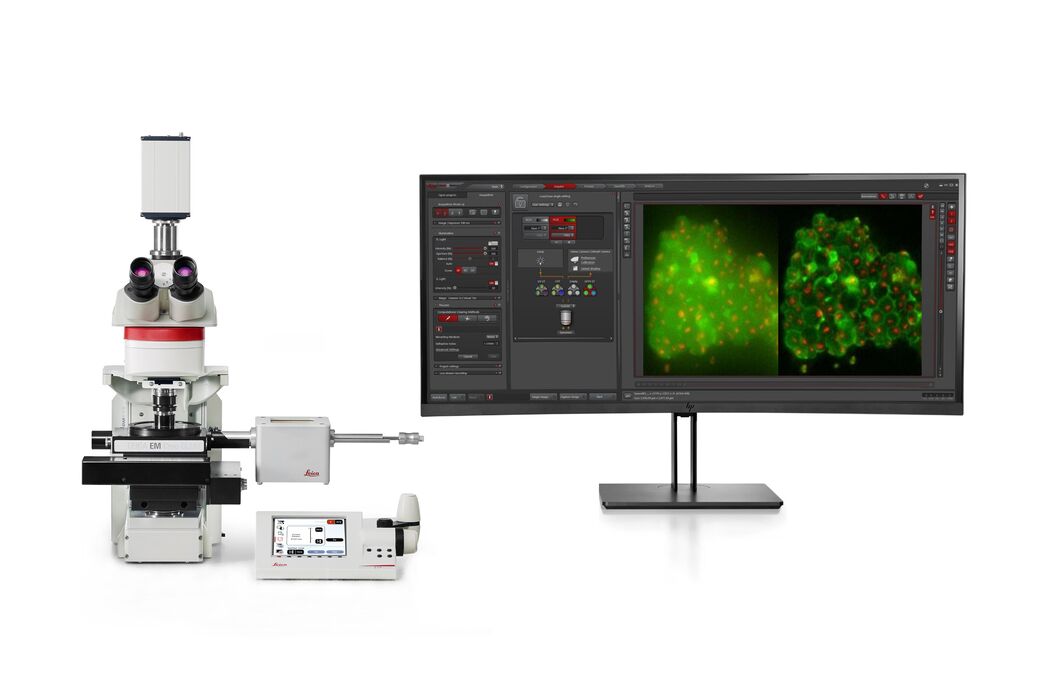
THUNDER Imager EM Cryo CLEM
THUNDER Imaging Systems
製品紹介
Home
Leica Microsystems
THUNDER Imager EM Cryo CLEM クライオ蛍光顕微鏡
細胞構造生物学に関する深い理解
アーカイブした製品
This item has been phased out and is no longer available. Please contact us to enquire about recent alternative products that may suit your needs.
THUNDER EM Cryo CLEMは、THUNDERイメージャーのオプトデジタル技術を搭載したクライオ蛍光顕微鏡です。 これは、細胞構造生物学に関する実験の成功のカギとなる画像データと安全なクライオ条件を提供します。 THUNDERの技術による高精細で蛍光ボケの無い画像から関心領域の細胞構造を正確に特定し、ユーザーの電子顕微鏡へシームレスに試料を移送します。
研究用途のみ