EM‑Probenvorbereitung: Typische Workflows und Anwendungen
Mit den Probenvorbereitungslösungen von Leica Microsystems können Forscher bei der Abbildung von Proben mit der Elektronenmikroskopie durchgängig hochwertige, präzise und reproduzierbare Ergebnisse erzielen. Unsere Lösungen unterstützen Rasterelektronenmikroskopie (REM), Transmissionselektronenmikroskopie (TEM) und Kryo-EM.
Unsere Imaging-Experten stehen Ihnen mit Rat und Tat zur Seite, wenn es um Lösungen für EM Sample Prep Workflows geht.
Wie können Forscher ihre Proben für REM vorbereiten?
Die Probenvorbereitung für die Rasterelektronenmikroskopie (REM) umfasst Techniken wie Beschichtung, Trocknung und Einbettung, um eine optimale Bildgebung zu gewährleisten. Mit den Lösungen von Leica Microsystems für REM-Proben verbessern Forscher die Leitfähigkeit, reduzieren Artefakte und sorgen für stabile, hochwertige Oberflächen für zuverlässige REM-Bilder bei Raumtemperatur.
Welche Methoden sind für die TEM-Probenvorbereitung am besten geeignet?
Die Probenvorbereitung für die TEM (Transmissionselektronenmikroskopie) erfordert ultradünne, artefaktfreie Schnitte, Sputterbeschichtung von EM-Grids sowie Kontrastierung, um eine detaillierte Visualisierung der Strukturen zu ermöglichen. Dank der Präzision und Zuverlässigkeit von Leica Instrumenten können Forschende hochauflösende TEM‑Bilder erzeugen.
Was ist bei der Vorbereitung von Kryo-EM-Proben wichtig?
Kryo-EM profitiert von der Vitrifizierung durch schnelles Einfrieren, um Strukturen in ihrem natürlichen Zustand zu erhalten.
Die Kryo-Präparationslösungen von Leica Microsystems - einschließlich fortschrittlicher Vitrifizierung und Beschichtung über ultradünne Schnitte und Kryo‑Planfräsen bis hin zu anpassbaren Kryo‑Transfer‑ und CLEM‑Workflows - unterstützen die Herstellung reproduzierbarer, kontaminationsfreier Proben. Sie tragen dazu bei, die nativen Strukturen zu erhalten, ermöglichen ein präzises Targeting und eine hochauflösende Kryo-EM-Bildgebung.
Warum sollten Sie sich bei der EM-Probenvorbereitung für Leica Instrumente und Lösungen entscheiden?

REM-Probenvorbereitung
Zu den Instrumenten für die REM-Präparation von Leica Microsystems gehören Hochvakuum-Sputterbeschichter und Kritisch-Punkt-Trockner. Diese Lösungen unterstützen eine hochwertige Oberflächenbildgebung. Darüber hinaus liefern die Instrumente von Leica Microsystems konsistente und zuverlässige Ergebnisse für Ihre REM-Studien.

TEM-Probenvorbereitung
Forscher können sich auf die Präzision und Zuverlässigkeit der TEM-Präparationslösungen von Leica Microsystems verlassen. Ultramikrotome und automatisierte Kontrastiersysteme sind essenziell für ultradünne Schnitte und hochaufgelöste EM‑Bildgebung. Die Sputterbeschichtung verbessert die Leitfähigkeit der Probe und die Qualität der EM‑Bildgebung.

Umfassende Kryo-EM-Probenvorbereitung
Leica Kryo‑Präparationssysteme wie Grid Plunger und Hochdruckgefriergeräte unterstützen schnelles Gefrieren und die Vitrifizierung für Kryo‑EM‑Anwendungen. Darüber hinaus bietet unser Probentransfersystem für Kryo‑Workflows flexible Transferoptionen für unterschiedlichste Proben. Durch den Schutz vor Kontamination unterstützt diese Option zuverlässige, detaillierte Kryo‑EM‑Analysen.
Häufig gestellte Fragen zur EM-Probenvorbereitung
Die Probenvorbereitung für die Elektronenmikroskopie (EM) beinhaltet mehrere Schlüsselschritte, die notwendig sind, um Proben zu stabilisieren, für die Elektronentransparenz vorzubereiten und einen optimalen Kontrast für hochauflösende EM‑Bilder zu erzielen:
- Fixierung zur Stabilisierung biologischer Strukturen mit chemischen oder kryogenen Methoden
- Wasserentzug oder schnelle Vitrifizierung der Probe in Kryo-Workflows
- Einbettung für ultradünne Schnitte oder das Aufbringen der Proben auf Träger oder Grids
- Herstellung von elektronentransparenten ultradünnen Schnitten
- Beschichtung oder Kontrastierung
- Transfer der Proben in das Elektronenmikroskop unter sauberen, kontrollierten Bedingungen, um Kontamination oder Erwärmung zu vermeiden.
Leica Microsystems bietet Lösungen für all diese Schritte, um reproduzierbare, qualitativ hochwertige Ergebnisse bei der REM-, TEM- und Kryo-EM-Bildgebung zu erzielen.
Leica Probenvorbereitungslösungen sind für REM‑, TEM‑ und Cryo‑EM‑Anwendungen geeignet und unterstützen Workflows zur Abbildung von Oberflächen und inneren Strukturen.
Die REM-Präparation umfasst typischerweise Fixierung, Dehydratisierung mit anschließender Kritischer‑Punkt‑Trocknung zum Schutz empfindlicher Strukturen sowie die Beschichtung mit dünnen leitfähigen Schichten wie Gold, Platin oder Kohlenstoff zur Optimierung der Oberflächenbildgebung. Leica Microsystems bietet Sputter- und Kohlenstoffbeschichtungssysteme sowie Kritisch-Punkt-Trockner an, die dazu beitragen, saubere, stabile und leitfähige Oberflächen für eine konsistente Datenqualität zu erzielen.
Die Beschichtung verbessert die Leitfähigkeit und verringert die Aufladung von nicht leitfähigen Proben, was das Signal-Rausch-Verhältnis und die Bildstabilität verbessert. Die Wahl der Sputter- oder Kohlenstoffbeschichtung hängt von der Art der Probe und den Abbildungszielen ab.
Die Kritische‑Punkt‑Trocknung entfernt Flüssigkeiten ohne Oberflächenspannungseffekte und erhält so empfindliche Mikrostrukturen, die bei der konventionellen Lufttrocknung verformen oder kollabieren könnten. Sie wird üblicherweise bei biologischen und porösen Materialien angewendet, die für das REM bestimmt sind.
Die Transmissionselektronenmikroskopie (TEM) erfordert elektronentransparente Proben. Kleine Partikel oder dünne Filme von <100 nm sind für die TEM ausreichend dünn, aber dickere Proben werden oft durch Ultramikrotomie in ultradünne Schnitte geschnitten. Darüber hinaus sind geeignete Kontrastierung und stabile Träger erforderlich, um innere Strukturen hochauflösend darzustellen. Ultramikrotome und automatische Kontrastiersysteme ermöglichen konsistente Schnitte im Nanometerbereich und einen zuverlässigen Kontrast.
Die Ultramikrotomie erzeugt Schnitte im Nanometermaßstab, sodass Elektronen mit minimaler Streuung die Probe durchdringen können und die innere Ultrastruktur sichtbar wird. Präzise Ultramikrotomie ist entscheidend, um eine gleichmäßige Schnittdicke und reproduzierbare Ergebnisse zu erzielen.
Die Kontrastierung erhöht den Kontrast spezifischer Strukturen, indem sie unterschiedlich mit den Bestandteilen der Probe interagiert. Automatisierte Systeme tragen dazu bei, Kontrastierungsprotokolle zu standardisieren und so zuverlässige sowie vergleichbare TEM‑Datensätze zu ermöglichen.
Kryo‑EM bewahrt native Strukturen durch schnelles Gefrieren und Vitrifizierung anstelle von chemischer Fixierung und Dehydratisierung. Der Workflow hält während Transfer und Bildgebung kryogene Bedingungen aufrecht, um Kontamination durch Eiskristalle und strukturelle Artefakte zu minimieren.
Tauchgefrieren eignet sich für die schnelle Vitrifizierung kleiner oder dünner Proben, während Hochdruckgefrieren die Eiskristallbildung in dickeren oder komplexeren Proben verhindert. Beide Methoden zielen darauf ab, den nativen Zustand für Kryo-EM zu erhalten.
Kryo‑Planfräsen ist ein kontrolliertes Trimmen bzw. Polieren von Oberflächen bei kryogenen Temperaturen, um Kontaminationen zu entfernen, Eisartefakte zu reduzieren und gezielt Regionen von Interesse freizulegen. Es trägt dazu bei, glattere Oberflächen für eine konsistente Kryo-EM-Bildgebung zu erzielen.
Beim ultradünnen Kryoschnitt wird die Kryo-Ultramikrotomie eingesetzt, um Schnitte von vitrifizierten Proben unter Beibehaltung der nativen Strukturen herzustellen. Es ermöglicht die Visualisierung der inneren Ultrastruktur unter kryogenen Bedingungen mit minimalen Artefakten.
Ein spezielles Kryo-Transfersystem sorgt für niedrige Temperaturen, schützt die Proben vor Umwelteinflüssen und reduziert das Kontaminationsrisiko während der gesamten Handhabung und des Transports, so dass die Integrität von der Vitrifizierung bis zur Bildgebung gewährleistet ist.
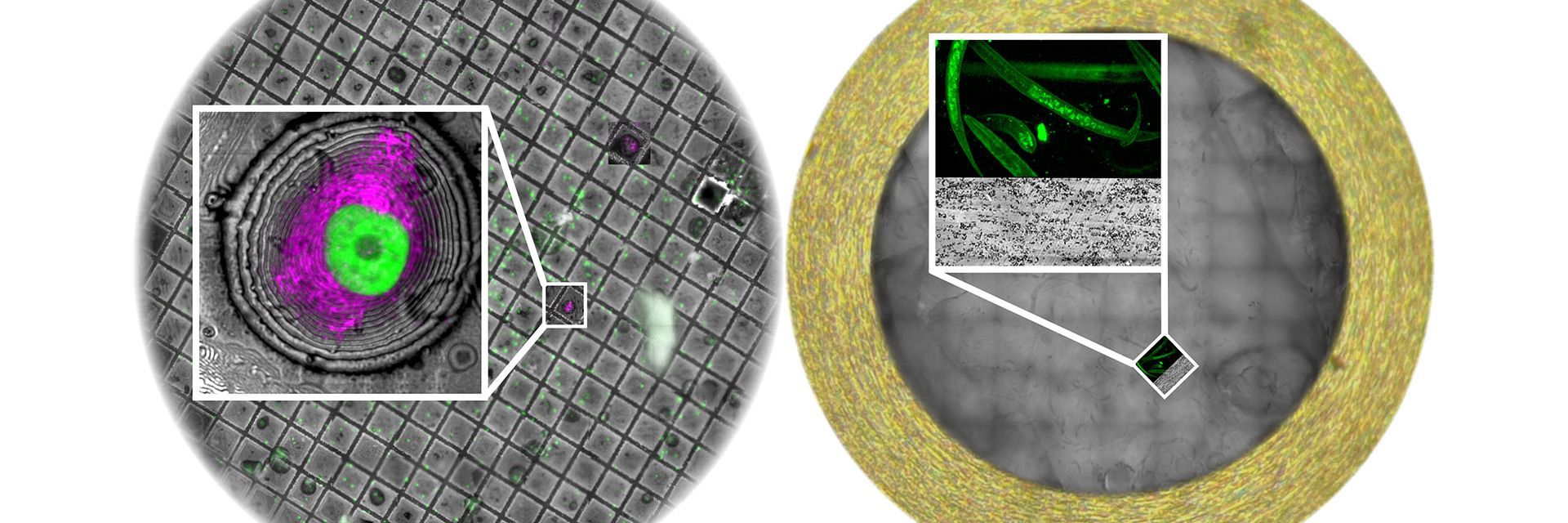
Die CLEM-Navigation korreliert Regionen, die in der Lichtmikroskopie (oft Fluoreszenz) identifiziert wurden, mit den genauen Koordinaten, die in der EM untersucht wurden. Sie ist besonders wertvoll, wenn funktionelle oder molekulare Signale aus der Lichtmikroskopie präzise mit der Ultrastruktur in der Elektronenmikroskopie korreliert werden müssen – auch in kryogenen Workflows.
REM eignet sich für die detaillierte Untersuchung der Oberflächenmorphologie, TEM für die hochauflösende Analyse der inneren Ultrastruktur und Cryo‑EM, wenn der Erhalt des nativen Zustands entscheidend ist. Die Entscheidung hängt von der biologischen Fragestellung, dem jeweiligen Probentyp und der benötigten Auflösung ab.